Por Javier Felcaro
Política
Rosario, uno de los próximos pasos de Mauricio Macri de cara a 2027

Negocios
Horacio Marín: "Quiero quedarme en YPF para desarrollar Vaca Muerta"

Por Claudio Berón
Policiales
El narco negocio de los Borras: avionetas, la DEA y cocaína por más de 15 millones de dólares

la ciudad
Domingo inestable y fresco en Rosario, la previa a una semana casi invernal

policiales
Zona sur: rescataron a un joven que estaba secuestrado y detuvieron al presunto captor

Por Matías Petisce
La Ciudad
Ciencia para todos: alumnos de la escuela Balseiro vivieron una experiencia "inolvidable" en el Xlab Rosario

La Ciudad
El Mundial cada vez más cerca, pero no los televisores: la venta en Rosario viene "floja"

Salud
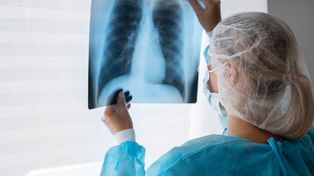
Cuadros respiratorios: con el frío intenso, aumentan las consultas en Rosario

Policiales
Zona oeste: encontraron a un hombre acribillado a balazos en el pasillo de una casa

La Ciudad
Docentes de la UNR lanzaron un nuevo paro de semana completa del 26 al 31 de mayo

La Ciudad
Un banco de Rosario sacó las cajas de seguridad a la calle y se alteró el microcentro

Por Luis Emilio Blanco
La Región
La Justicia Federal consolidó pruebas clave en el juicio por fumigaciones en Pergamino

La Ciudad
Un simple botón: cómo hacer que La Capital aparezca primero en tus búsquedas de Google

Política
El rector de la UNR criticó a Javier Milei por haberlo llamado "delincuente"

La Región
La ruta 34 sumó otro choque fatal: un automovilista de San Lorenzo murió en Ybarlucea

La Región
Santa Fe lidera el ranking de puestos de trabajo en la construcción con saldo a favor

Policiales
El MPA presentó su informe sobre crímenes en Rosario y destacó la tasa de esclarecimiento

Por Jorge Asís
En foco
Derecha módica o peronismo resignificado

la ciudad
El fin de semana será gris e inestable antes del ingreso de un nuevo frente frío

Policiales
Crimen de Benjamín: el rumor que llevó al hallazgo del cuerpo tras una semana sin novedades